������ ± ��
4.1 �� ��
�ӹ����Ͻ������л������������̼ԭ��������±��ԭ�ӵķ�Ӧ��������±����������������ӵIJ�ͬ���ɷ�Ϊ�������Ȼ����廯���⻯�ȡ�
±���Ǿ�ϸ�л��ϳ�������Ҫ�ķ�Ӧ֮һ���ڴ��ģ��ҵ�����У����������Ⱥͷ����л����壨������ϩ���ķ���ϩ���Լ��л��ܼ������Ȼ�̼���������顢�ȱ��ȣ���������������������⣬�ھ�ϸ�л������У����㷺������ȡũҩ��ҽҩ�����ܼ������͡���ȼ����Ⱦ�ϡ������Լ����ϻ����Ȳ�Ʒ���м��塣
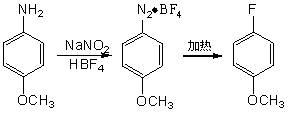
���л����������������±�ص�Ŀ����������һ��Ϊ�˵õ�������������ղ�Ʒ�����磺��Ⱦ�Ϸ����к���±��ԭ�ӣ����Ը���Ⱦ�ϵ�ijЩ���ܣ���ijЩ�л�������������±��ԭ�ӣ����������л������ȼ�ԡ���һĿ���ǿ��Խ��Ȼ����ò�Ʒ��ͨ����һ��ת�����Ʊ������м����Ʒ�����磺
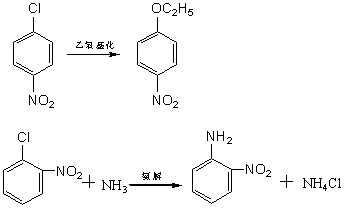
4.2 �����ϵ�ȡ��±����Ӧ
4.2.1 ��Ӧ����
������ȡ��±���ķ�ӦͨʽΪ��ArH + X2 = ArX + HX
�����ϵ�ȡ��±����Ӧ���ǵ��͵���ȡ����Ӧ�����������Ļ����ʵ㣬����±������(X+)������ʹ��ʲô���͵Ĵ��������ǵ����ö��Ǵ�ʹ±������(X+)���γɡ�
4.2.1.1 �Խ���±����Ϊ�����ķ�Ӧ����
�Խ���±����Ϊ������±����Ӧ���ڹ�ҵ������Ӧ����㷺�����õ�±������FeCl3��A1Cl3��ZnCl2���ȡ����ǵĴ���Ӧ��������FeCl3���Ȼ�Ϊ��������±��������ǿ���ԣ���ʹ�ȷ��Ӽ�����������������(Cl+)��
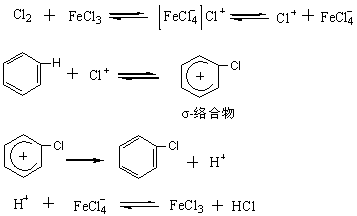
��Ӧ���̲������Ĵ�������˴����������١��Ա����Ȼ�Ϊ����FeCl3�����Ϊԭ���������֮һ���㹻�ˡ������ϱ���������Ч�Ĵ������������Ȼ�����һˮ����(FeCl3��H2O)�������ߵķ��ӱ�(FeCl3�UH2O)Ϊlʱ����Ӧ�ٶȳ���Ϊ���ֵ������1ʱ����Ӧ�ٶȳ�����С����ˣ����Ȼ���Ӧ�У�ԭ�Ϻ�����ˮ��(���뱣��FeCl3�UH2O��1)���������ɸ��ϴ������ܼ��ٷ�Ӧ�Ľ��С�
4.2.1.2 ������Ϊ�����ķ�Ӧ����
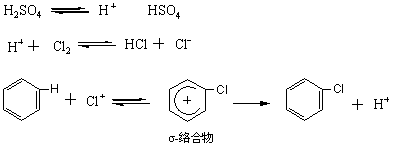
4.2.1.3 �Ե�Ϊ�����ķ�Ӧ����
�Ե�Ϊ������ͨ���Ȼ���ֽ���ĵ����������������ã���ʹ������������(Cl+)���Ȼ���(ICl)���Դ˷������С�
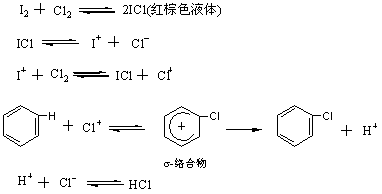
4.2.1.4 �Դ�±��Ϊ�����ķ�Ӧ����
���෴Ӧ���̣�������Ϊ�Ƿ�Ӧ�������Ӵ��ڣ���ʹ����±�����Ӷ������˷�Ӧ�Ľ��С�
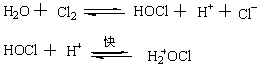

���ڱ����ϵ�ȡ���Ȼ���Ӧ�ǵ��͵���ȡ����Ӧ����ˣ��������������ӻ��Ŵ���ʱ����Ӧ���ѽ��У�����Ҫ��������������������и����ӻ���ʱ����Ӧ�����У��е��������Բ���Ҫ���������磬���ࡢ���༰����������Ȼ��������ȷ��ӱ������ܵ������ļ������ܹ�˳�����з�Ӧ���䷴Ӧ���̿���Ϊ�ǣ�
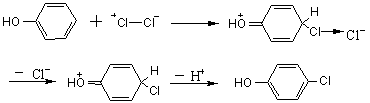
4.2.1.5 �廯�ķ�Ӧ����
�廯�ķ�Ӧ�������Ȼ�������ͬ��������������þ��п�Ƚ������廯���⡣�廯ʱ�����������������������ơ��������Ƶȣ���������Ӧ�����ɵ��廯�⣬�Գ���������ء�
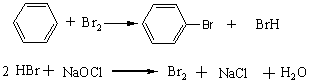
4.2.2 ��Ӧ����ѧ
�����ϵ��Ȼ���Ӧ����������Ӧ������һ����Ӧ��������������һ����Ӧ�ķ�Ӧ��Դ����������еķ�Ӧ�����籽���Ȼ���

������±��ȡ����Ӧ������ȡ����Ӧ������ȡ���˷����ϵ���ԭ���Ժ���Ȼ�������ͻǻ���Ӧһ������ʹ�����ۻ������Ȼ�ͬʱ�����������ӵ���������ˣ��ۻ��ij̶�ԶԶС�������ͻ������Ҳ����˵���ڷ�����±����Ӧ�У�һ±�������ڲ������ȡ����Ӧ�Ծ����൱�Ļ����ԣ�ʹ��±����Ӧ�Ƚ������С����±��п�֪��
�����������ǻ����Ȼ���k1/k2ֵ�ıȽ�
|
��Ӧ���� |
���� |
�ǻ� |
�Ȼ� |
|
k1�Uk2 |
105~107 |
103~104 |
~101 |
����һ�Ȼ����ȱ��Ľ�һ���Ȼ���Ӧ���ٶȳ������ֻ��10�����ҡ�ʵ��֤������±����Ӧ�У����ŷ�Ӧ������Ũ�ȵIJ��ϱ仯��ʹ������Ӧ�ķ�Ӧ����Ҳ��Ӧ�����ϴ�ı仯�����磬�ڱ����Ȼ��У������е��ȱ�����Ϊ1%��������ʱ��һ�Ȼ��ٶȱȶ��Ȼ��ٶ�Լ��842���� �����е��ȱ�����Ϊ73.5%��������ʱ�������ٶȼ�����ȡ�Ҳ����˵���ڱ����Ȼ��У�����һ�ȱ��IJ������ɣ����Ȼ���Ӧ�ٶȲ������ӣ��������ɽ϶�Ķ��Ȼ��P���Ȼ��
4.2.3 Ӱ�����ؼ���Ӧ������ѡ��
4.2.3.1 �Ȼ���ȵ�Ӱ��
�ӱ�4-1�п��Կ����������Ȼ���Ӧ���������ǻ���Ӧ��k1��k2�ıȽϣ�����������������һ�Ȼ���Ӧ�ٶȳ������ڳ����½��ȶ��Ȼ���8.5�����ҡ����Ҫ����һ�Ȼ��������ɶ��Ȼ���ͱ����ϸ�����Ȼ���ȡ��Ӷ���ѧ�о�����ͼ������Կ���������Xֵ�����ӣ�����ת�������ӣ�һ�ȱ��ĺ�����Ȼ�������ӣ������ȱ��ĺ���Ҳ��֮���ӡ�
���ڼ�Ъ�Ȼ�ʱ�IJ�����ɱ仯
4.2.3.2 ������õ�Ӱ��
�ڱ����Ȼ���Ӧ�У��������Ч�����û�Է�Ӧ����ʽѡ�������ʲ��ȣ�ʹ��Ӧ���ɵIJ���δ�ܼ�ʱ�뿪���ַ��ص���Ӧ����ٽ�������Ӧ�Ľ��У���������Ϊ�������á�һ�ȱ����������վ��������εı���ʼ�ǵ�����Ъʽ����(ͼ4-2a)��Ϊ���������Ч�ʣ���չΪ��������Ȼ�(ͼ4-2b)���������������з������������ַ�չΪ��ʽ����������Ӧ(ͼ4-2c)��

4.2.3.3 ��Ӧ�¶ȵ�Ӱ��
������֪��һ�㷴Ӧ�¶�Խ�ߣ���Ӧ�ٶ�Խ�졣���ѽ��еķ�Ӧ�������¶ȵ����ӷ�Ӧ�ٶ��������ӡ��ӱ�4-4���Կ�������ȡ���Ȼ���Ӧ�У����Ȼ���Ӧ���ٶȣ������¶ȵ����ӣ���һ�Ȼ��������졣�����ڵ��ȱ������У�Ϊ�˷�ֹ���ȱ����ɹ��࣬�����ܿ��Ʒ�Ӧ��35~40���½��С��������Ȼ���Ӧ��ǿ�ҷ��ȷ�Ӧ��ÿ����1mol�ȱ����ų���Լ131.5kJ(31.4kcal)����������ˣ�Ҫά���ڵ��·�Ӧ����Ӧ����Ҫ�ϴ����ȴϵͳ������������������ܵ������ơ�ͨ���о����֣������¶ȵ����ߣ�k1/k2���ӵIJ���ʮ���������¶ȵ�Ӱ��ȷ������õ�Ӱ��ҪС�öࡣ��ˣ��ڽ�����һ�ȱ������У��ձ�������Ȼ�Һ�ķ����¶��£�78~80�棩������ʽ��Ӧ�������й�ʽ�Ȼ������з�Ӧ���������������ɴ��߷�Ӧ�ȣ����ڿ��Ʒ�Ӧ�¶ȣ�����������������������ʹ���������������ߡ�
����������Ӧ�¶���k1/k2�Ĺ�ϵ
|
T�� |
18�� |
25�� |
30�� |
|
k1/k2 |
0.107 |
0.118 |
0.123 |
4.2.3.4 ԭ�ϴ��ȵ�Ӱ��
�ڱ����Ȼ���Ӧ�У�һ�㲻ϣ��ԭ���к����������ʣ��ر�����ԡ���Ϊ��������������ã����ɺ�ɫ������ʹ����ʧЧ�����ң����ɵIJ����ھ����У��ֻ�ų��Ȼ������壬��ʴ��������
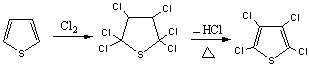
��ˣ��������������л��յı������Ȼ�ǰ����ȳ�ȥ�л�������⣬���л�ԭ���л���ϣ������ˮ�֡���Ϊˮ�뷴Ӧ���ɵ��Ȼ��������������ᣬ���Դ������Ȼ������ܽ�ȴ���л�������Ȼ������ܽ�ȡ�ˮ�Ĵ��ڻ����л����д������Ȼ�����Ũ�ȣ�ʹ��Ӧ�ٶȼ�����ʵ��֤�������еĺ�ˮ������ǧ��֮��ʱ���Ȼ���Ӧ�����ܽ��С����⣬Ϊ�˱���������ֻ�ը�¹ʣ�Ҫ���Ȼ��������к���������4%����һ�ȱ������У����ڱ��ȱ�ԼΪ4�U1�������ı�Ҫ������������ѭ���������ϣ�����ɹ���Ķ��Ȼ��Ӧ��ǿ���շ��룬ʹѭ�����е�һ�ȱ�����Խ��Խ�á�
4.2.3.5 ������ѡ��
�����ϵ�ȡ��±����Ӧ��һ����ȡ����Ӧ������ڷ����ϴ��н�ǿ�Ĺ����ӻ��ţ����ǻ�������������±��ʱһ��ɲ��ô������Ի����Խϵ͵ķ�������ױ��������ȱ�����±����һ��Ҫ�������±�������������Բ����õķ������������ȣ���ֱ��±������Ҫ����ǿ�ҵ�±�������ʹ�����һ�����Ũ���ᡢ����Ȼ�����Ϊ��������һЩ�����������ı��칹����ɵ����á����ڱ��Ȼ���ȡ���ȱ�ʱ�������ʵ��Ķ������������������࣬����ʹ��-���ȱ��õ��ϸߵ����ʡ�
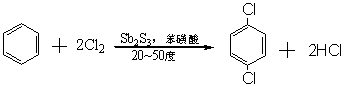
4.2.l.6 ��Ӧ���ʵ�ѡ��
±����Ӧ���ݱ�±��������ʲ�ͬ��Ҫ��ѡȡ�ķ�Ӧ����Ҳ��ͬ���ڷ�Ӧ�¶���ΪҺ̬�ķ����������ڴ������������£�ֱ�ӽ���±����Ӧ��һ�㲻����������Ӧ���ʣ��������Ϊ���Է�Ӧ�ﱾ��Ϊ���ʶ�ֱ��±�����籽���ױ������������Ȼ�������ڷ�Ӧ�¶��£���Ӧ���ǹ�̬�ģ��������ʽ�Ϊ���ã�һ��ɽ�����ɢ��ˮ�����������������������½���±�������磬�������������Ȼ��������������廯��1-��������-������廯������ڷ�Ӧ�¶��£���Ӧ���ǹ��壬�ұȽ���±������������Ҫ�ܽ���Ũ���ᡢ����������Ȼ�������н���±������ʱ��Ҫ�õ��������������������Ȼ�������һЩ�����������ױ�±�����л����Ϊ�ܼ�����±������ˮ�������ȱ�������е��Ȼ���
4.2.4 �ȱ�������
�ȱ�����ȡũҩ��ҽҩ��Ⱦ�ϡ������������л��ϳɲ�Ʒ����Ҫ�м��壬Ҳ����ֱ�����ܼ�������ȫ����������������ɴ���ʮ��֡��ȱ�������·����������һ�DZ���ֱ�Ӵ��Ȼ�������
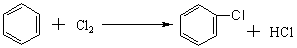
��һ�DZ��������Ȼ������ɱ����Ȼ���������ڸ��´������·�Ӧ���Ƶá�����·�������ڱ��ӵ�������δ����������Ϊ�ȱ���������
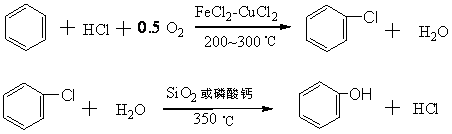
����ֱ�Ӵ��Ȼ���������������ͼ4-3��ʾ�������IJ����������£�����������ʳ�θ���ı��������������ȱ�Լ4��l��Ħ���ȣ��ı�������������������ϣ������������Ȼ����ײ���ά����75~80��֮�䣬ʹ���ڷ���״̬�½��з�Ӧ���Ӷ����ų��ı��������Ȼ������壬��ʯī����������������Һ�����ᱽ���������룬������ı��������ڣ����������Ȼ���ȥ����ϵͳ����ˮ���յõ����ᡣ�ӷ�Ӧ���϶��������ķ�ӦҺ�У�Ҫ����������ӦҺ����Һ��ۣ�������ʯī��ȴ����ȴ����ȥˮϴ���к͡����롢�����ɷֱ�õ���Ʒ�ȱ������ȱ������յ�ԭ�ϱ���
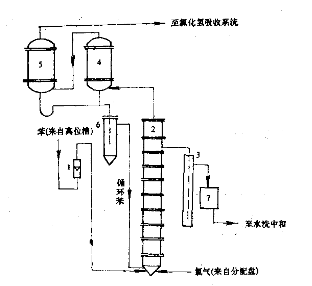
�ȱ�������������ͼ
1-�����ƣ�2-�Ȼ�����3-Һ������4,5-��������6-�ᱽ��������7-��ȴ��
4.2.6 �����ϵ��廯�͵⻯
�����ϵ��廯���Ȼ���Ӧ�����̡����ô�����ʮ�����ơ����������Դ����Ȼ���б����ٵö࣬�۸�Ҳ�ȽϹ�Ϊ�����廯��Ӧ�г���������أ����������������̣�ʹ���ɵ��廯���ٱ����������أ����Գ�����á����õ��������д������ơ������ơ�˫��ˮ��������
�ھ�ϸ�л��ϳ��У��������廯��Ӧ�У�
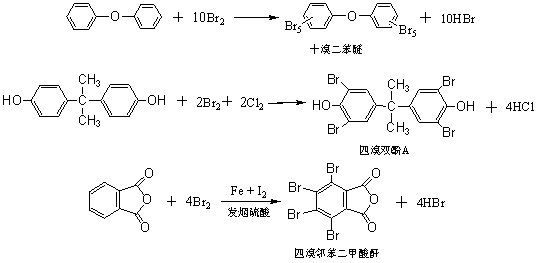
���������������������ά��������Ʒ�У���Ϊ��ȼ����Ӧ�õõ��˺ܴ�ķ�չ��Ŀǰ���������廯��ϵ����ȼ����ʹ�����������ڹ�ȥ���������Ȼ���ϵ����ȼ�����廯��ϵ����ȼ������Ҫ������˫��A��ʮ������ѣ��۶��屽�ѣ������ڱ�����������������ȡ����磺
 4.3 ֬��������������ȡ��±��
4.3 ֬��������������ȡ��±��
4.3.1 ��Ӧ����
֬��������������ȡ��±����Ӧ�������������Ӧ���Ǿ�ϸ�л��ϳ�����Ҫ��Ӧ֮һ�����෴Ӧһ��ֳ������Ρ�
4.3.1.1 ���������
Ϊ��ʹ�������Ӧ��˳�����У����ȱ������һ�������������������������ķ��������֣��������ѽ⡢�����͵���ת�Ʒ���
1. ���ѽⷨ
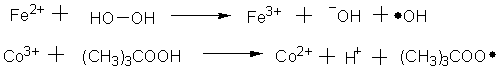
�����������ڸ������ܷ������ѷֽ⡣��500~650��Է��ӽ����ȼ���������ʹC-C��C-H��H-H�����Ĺ��ۼ����ѷֽ⡣��Ϊ��Щ���������ԼΪ330~418.6kJ/mol (80~100kcal/mol)����C1-C1��Br-Br��I-I��O-O��N-N��C-N=N-C��������ܽ���250kJ/mol (60kcal/mol) ���¡�������50~150����¶ȷ�Χ�ڼ��ɽ������ѽ⣬�Ӷ��ṩ�����ɻ�����Դ�����磺

����һЩ�ڵ������������ѽ���������������ʣ����������������ż�����춡��ȳ�֮Ϊ������������������£��������������ѽ����������������������Ӧ��
2. ����ⷨ
��������ܵ���������������յ����������������������ⷽ������֮Ϊ����ⷨ����Ϊ���ɼ��Ⲩ��400~500nm֮��Ĺ���������250kJ/mol���ϣ�������400nm�Ⲩ�Ĺ������ܸ�ǿ��ʹ�����ֲ����Ĺ⣬����Cl2��Br2��I2���ӣ�һ�����չ��ܣ�ͬ���ܷ������Ѷ������������

3. ����ת�Ʒ�
�ؽ������Ӿ��е�ʧ���ӵ����ܣ����dz��������ڴ�ijЩ��������ķֽ⡣���磬�������ӽ�һ������ת�Ƹ��������⣬ʹ������һ���ǻ��������һ�����ȶ����ǻ������ӡ�����������Ҳ���Դӹ������嶡���л�ȡһ�����ӣ���ʹ�������嶡��ת���һ�������������һ�����ӡ�
4.3.1.2 ��Ӧ���Ĵ���
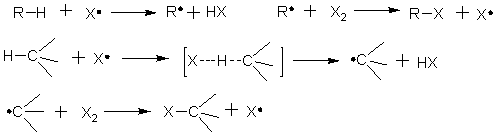
ͨ���ѽ���������������������Ѹ�ٰ����з�ʽ�����������������Ӧ��
�����Ĵ���������ÿ��һ��������μӷ�Ӧ��������һ���µ����������˷���ѭ�����ɴXǧ����������Ρ�
4.3.1.3 ��Ӧ������ֹ
�����ѭ�����Ĵ��ݣ���ʵ���ϣ�����������ѭ����ȥ���ܻ�����ijЩ���صĴ��ڶ���ֹ�����磬�������������ײ���ͷų������������ϣ�����ijЩ��ֹ�����軯�����Ĵ����£����������������ʣ������������ֹ�������ȶ��Ļ�������õ��ʵ㣬�Ӷ�ʹ��Ӧ���жϡ�
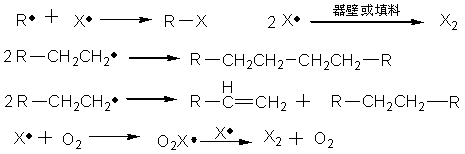
4.3.2 Ӱ������
4.3.2.1 �����������¶ȵ�Ӱ��
�������Ӧ�����Ŀ���ȡ�������������������������������������������Ϊ�����������ϸߣ���������������������Ȼ�Ϊ�����ȷ��ڵĹ⻯�������250kJ/mol(59.7kcal/mol)����ʹ�ȷ��ӷ����⻯����������ó���478.5nm����IJ���Խ�̣���������Խǿ��������С��300nm������⣬��������ͨ�����������ڹ�ҵ�����У������ø����������չ�ƹ�Դ�����䣬�䲨����Χ��400~700nm֮�䡣
4.3.2.2 ���������ʵ�Ӱ��
��Ϊ����������������±�����ϩ���ͷ����ļӳ�±�����ϵ���ȡ��±���������������н���±��������£��������������Ӧ��������������ֹ�������Ӧ�Ľ��С��ӷ�Ӧ����ѧ�о��з��֣���±����Ӧ�У�����д����Ĵ��ڣ�����Ӧ���ٶȴ������������Ӧ���ٶȡ���ˣ�ͨ���������Ӧ���з���������±��ʱ����Ӧ�豸��������ͨ���豸����Ҫ�óIJ������´ɻ�ʯī��Ӧ�������ң�ԭ����Ҳ���ܺ�����������
�������ʵĴ��ڣ��������к�������������Ҳ�����Ʒ�Ӧ�Ľ��С���Ϊ������������δ�ɶԵ��ӣ�����˫����������ʣ���O��O������������߶Ȼ��õ��������ϣ��Ӷ�ʹ������Ӧ��ֹ��
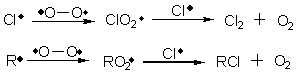
4.3.2.3 �Ȼ���ȵ�Ӱ��
�����ȡ����ӦҲ��һ��������Ӧ����ֱ���Ȼ��ķ������������Ƶõ�һ���Ȼ�������Ȼ���Ӧ�У���Ʒ����������Ȼ���Ӧ��ȵı仯���仯���Ȼ����Խ�ߣ����Ȼ������Խ�ߡ�������Ҫһ�Ȼ����Ʒ�����ϸ���Ʒ�Ӧ���Ȼ���Ȼ�ԭ�ϵı�����Ҳ��ʮ�ֱ�Ҫ�ġ�
4.3.3 �Ȼ��е�����
�ױ��IJ����Ȼ�������ȡ�Ȼ���
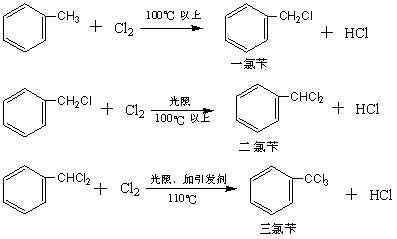
����������һ���´ɸ����²�����ʽ��Ӧ���н��С�������������Ҫ�ڲ����������չ�����䡣���������г����ȡ����������뷼������0.01~0.1%������������110�����Ϸ��������·�Ӧ���ڹ�ҵ�����У��ÿ���ͨ�Ⱥ�ӦŨ������ܶ��������Ȼ���ȣ�������ױ���Ħ���ȣ����Դ���������ͬ�Ȼ��̶ȵIJ�Ʒ��
4.4 �ӳ�±��
���üӳ�±�����ԴӾ���˫����������ijЩ�������л�����������ȡ±���顢±��ϩ����±�����������ӳ�±������±�ض�˫���ļӳɡ�±�����˫���ļӳɣ�������±�����˫���ļӳɡ�
4.4.1 ±�ض�˫���ļӳ�
±�ض�˫���ļӳɷ�Ӧ����Ҫ�����ֲ�ͬ�ķ�Ӧ���̡�����ӳɺ�������ӳɡ�
4.4.1.1 ��ӳ�±��
��ӳ�±��һ�㾭��������������±�ط��Ӷ�˫�������繥�����γɹ���̬�ġ���-������Ȼ����·��ʿ������������Ȼ������������£�����±������·��ʿ������ã��������ڼ�����-�����ת��Ϊ��-�������һ�����ʹC12������γ�Cl-Cl�UFeCl3�����������������������磺
 ϩ���ķ�Ӧ������ȡ�����м��������ӵ��ȶ��ԣ�����ô������£�
ϩ���ķ�Ӧ������ȡ�����м��������ӵ��ȶ��ԣ�����ô������£�
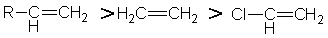
��±�ص���ӳɷ�Ӧ�У�һ����õ��ܼ������Ȼ�̼���ȷ¡�����̼������ȡ����Դ���ˮ��Ϊ�ܼ����������ǿ���Ϊ���Լ��������̬��-��������˽��������ܻᷢ������±������±���ѵĸ���Ӧ����±����ӳɷ�Ӧ�У���Ӧ�¶Ȳ���̫�ߣ���������ȥ±����Ŀ��ܣ�����ͬʱ����ȡ������Ӧ��
4.4.1.2 ������ӳ�±��
������ӳ�±����±�����ڹ�ļ���������¡������������Ĵ����£���������±ԭ���������Ȼ����˫�������ӳɷ�Ӧ���䷴Ӧ�����ǣ�

��±���ӳɵķ�Ӧ�ر�������˫�����������ӻ���ϩ��������������ϩ����������ԭ�ӣ���һ���ӳ��Ȼ������ѣ����ù���Ȼ�������ȡ�������顣�������龭����һ���ӵ��Ȼ�����Ƶ��������ҩ��������ϩ��
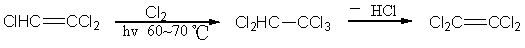
������ӳ�±����Ӱ������ȡ�������뵴����������ֹ��
��������ĺϳ�Ҳ��һ�����͵�±�ؼӳɷ�Ӧ�����������ǵ���ɫ����ȼҺ�壬�������Ժ͵�µij�ζ����ˮ�أ�������ˮ��������ҽҩ��Ⱦ�ϵ��м��壬Ҳ������ȡ������Ѭ���������ȡ���������ĺϳ��ǽ����غ���Ȳ��һ����������ͨ�����ڣ���Ӧ�¶���58~62���½��мӳɷ�Ӧ��
4.2 ±�����˫���ļӳ�
±�����˫���ļӳɷ�Ӧ�Ƿ��ȵĿ��淴Ӧ����Ӧ�¶����ߣ�ƽ�������ƶ����¶Ƚ��ͶԼӳɷ�Ӧ����������50�淴Ӧʱ����Ӧ���������档±����ļӳɷ�ӦҲ�����࣬����ӳɺ�������ӳɷ�Ӧ��
4.4.2.1 ±�������ӳ�
±������̼��̼˫���ļӳɣ��Ƿ��������еġ����������ӶԷ��ӽ�����������ڶ�������һ��±�������

�ڷ�Ӧ�м���·��ʿ�ᣨA1Cl3��FeCl3������ʹ��Ӧ�ٶȼӿ졣����
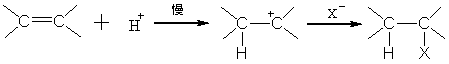
��������ӳɷ�Ӧ����ԭ�Ӻ�±ԭ�ӵĶ�λ���ɷ��������Ʒ���Ʒ������ԭ�Ӽӵ�����ԭ�Ӷ��̼ԭ���ϣ���ϩ���и����ӻ�ʱ���Է�Ӧ��������ϩ���ϴ���ǿ��������ȡ��������-COOH��-CN��-CF3��-N+(CH3)3ʱ��ʹϩ�����������Ƽ�ȡ��������ת�ƣ���±����ӳ�ʱ���Ӽӵ����и���ɵ��Ǽ�̼ԭ���ϣ���±�ؼӵ���������ɵ��Ǽ�̼ԭ���ϡ���ˣ����ǵļӳɷ������������Ʒ���Ʒ�����෴��

4.4.2.2 ±�����������ӳ�
�廯����ϩ�����ڹ��ջ��������Ĵ����½��мӳɷ�Ӧ����ǰ�治ͬ������������ӳɷ�Ӧ����ˣ�Ӧ��ע���䶨λ�����������Ʒ���Ʒ�����෴�����磺

4.4.3 ����±�����˫���ļӳ�
��˫���ӳɵ�±��������±�������⣬���д�±�ᡢN-±��������±�顣����������˫���ļӳɷ�Ӧ������ӳɷ�Ӧ����һ�������������������������ᡢ·��ʿ�������ʹ��Ӧ���١�
4.4.3.1 ������ļӳ�
������ˮ��Һ����ϩ���ϩ�ļӳ���ʮ�ֵ��͵����ӡ����ɵ���-���Ҵ����ȱ�������ʮ����Ҫ���л�����ԭ�ϣ���������ȡ��������ͻ������顣��Ȼ����ȡ��������Ĺ����ֽ��ѱ���ϩ��ֱ������ȡ�������ô��������ϩ�ӳɵĹ����������������飬������ʮ����Ҫ����ġ��ò�Ʒ�������ܲ����ѳ���250��֣��ֶ����ô˹���·���������䷴Ӧ����Ϊ
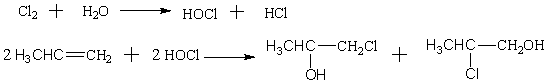
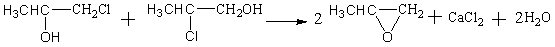 �������������ڷ�Ӧ���ڣ���ϩ�뺬��ˮ��Һ��35~50��֮�䷴Ӧ����ˮ��Һ�У�HCl��HOCl��ƽ��ġ���Ӧ���ɵ�4~6% ��-����-�ȱ�������9��1�����Բ������룬�ù����ļ��10%��ʯ���飩��25������HCl����Ӧ����ֱ������Ѹ�ٽ����������������Ա����һ������ˮ�Ϸ�Ӧ�����ʿɴ�87~90%������Ӧ��������������1,2-���ȱ���Ͷ��ȶ�������ѡ�
�������������ڷ�Ӧ���ڣ���ϩ�뺬��ˮ��Һ��35~50��֮�䷴Ӧ����ˮ��Һ�У�HCl��HOCl��ƽ��ġ���Ӧ���ɵ�4~6% ��-����-�ȱ�������9��1�����Բ������룬�ù����ļ��10%��ʯ���飩��25������HCl����Ӧ����ֱ������Ѹ�ٽ����������������Ա����һ������ˮ�Ϸ�Ӧ�����ʿɴ�87~90%������Ӧ��������������1,2-���ȱ���Ͷ��ȶ�������ѡ�
4.4.3.2 ��±����ļӳ�
±�����˫���ļӳɣ�������±������·��ʿ��Ĵ��£���˫��������������õ��ӳɻ������±������������Ҳ������˫������������ӳɷ�Ӧ��
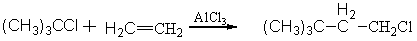
4.5 �û�±��
±ԭ���û��л������е��������ţ�����ԭ�ӣ��ķ�Ӧ����֮Ϊ�û�±����Ӧ�������Ӧ���ص������칹�����������±������Ʒ���ȸߣ�����ֱ��ȡ��±���IJ���ࡣ���ڲ�Ʒ���ȸߣ������ڹ�ҵ��������Ȼ����ʮ����Ҫ�ĵ�λ���ر�������ҩ��Ⱦ�Ϲ�ҵ��Ӧ�ý϶ࡣ
���û�±����Ӧ�У��ɱ��û���ȡ������Ҫ���ǻ�����������������ص��������������û�����±�������ҷ�����Ӧ��Ҫ��ͨ���û���Ӧ����ɵġ�
4.5.1 ±���û��ǻ�
±���û��ǻ��ķ�Ӧ���Ʊ�±�������Ҫ����֮һ������±������±���⡢����±����ͺ���±���
4.5.1.1 ��±����Դ��ǻ����û�

±����Դ��ǻ����û������û���Ӧ���䷴Ӧ�������£�
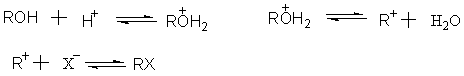
��ˣ����ǻ��Ļ��Դ�СΪ�� ���ǻ������ǻ������ǻ���
±�������ӵ���������С�Ĺ���Ϊ��HI��HBr��HCl��HF
�����ǿ��淴Ӧ��������Ӵ���±�����Ũ�Ȳ�������ȥ��������ɵ�ˮ�������ڼ��ٷ�Ӧ��������ʡ����ڵ�̼�����û���Ҫ�д����Ĵ��ڡ����磺

����Ũ�����Ƿ�Ӧ��Ҳ�Ǵ��������û���±�������У��еĴ�����ʹ�����ӻ������ٷ�Ӧ�Ľ��У�����ZnCl2��
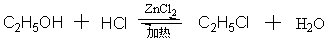
4.5.1.2 ��±��������±�����ǻ����û�
��±�������±�����ǻ����û��������ڶԸ�̼�����ӻ��ӻ��ǻ����û���Ӧ�����磺

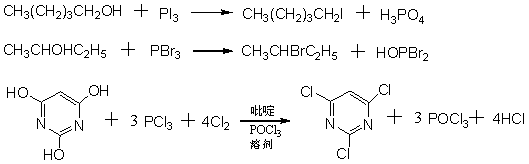
4.5.2 ±���û������
�������ϵĻ����ʮ�����ױ��Ȼ��û������ڹ�ҵ�������Ʊ�1-��������1,5-�������������磺
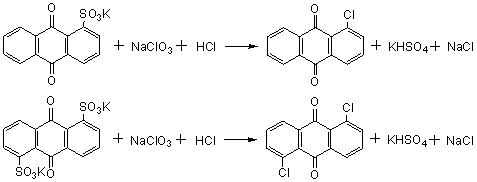
���ڲ�ͬλ�õ��ȴ��������в�ͬ���۵㣬��±���û��������ϵĻ�����ķ�Ӧ�����Ƕ������еģ���ˣ�Ҳ����Ϊ������������ķ���֮һ��
4.5.3 �û�����
���ڷ��ļ��Ժ�ǿ�����Է����Ӻ��ѱ���������������ɷ�������ʮ�����ѣ�������ȡ���������������������ӱȽϻ��ã���������������������л������ʮ�ּ��ҵ��������Ӧ���ų������������������������ϼ����ƻ��ȸ���Ӧ����Ӧʮ�ָ��ӣ����Կ��ơ���ˣ�ֱ�ӷ������з�����ը��Σ�ա�Ϊ����ȡ����ķ����һ�㶼�����û������ķ�������HF��KF��NaF��AgF2��SbF6�ȷ������û��л��Ȼ����е��Ȼ����Ʊ���Ӧ�ķ�����ڹ�ҵ������ʹ��������HF��NaF�������䷴Ӧ���Ա�KF��AgF2�ͣ���������ã����Թ�Ϊʹ�á����磺
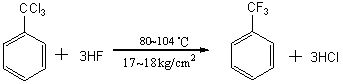
��������ﰺϵ�в�Ʒ������һ����ͨ���û������Ƶõġ����磺
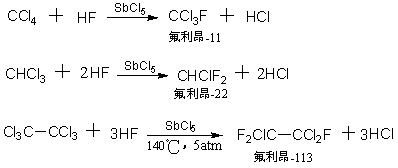
���ﰺ-22������ȡ���������ķ���ϩ�������Ҫԭ�ϣ�
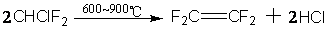
����������������������⣬����ͨ���ص���ת���ķ���������������磺