��ʮ���� ��
��������ȡ�����Ϊ�������ݰ�����������ȡ���ĸ���������ɷ�Ϊ��

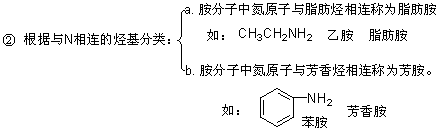
������뼾識��Σ�  ����
���� 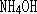 �е��ĸ���ԭ�ӱ�����ȡ�������ɵĻ������Ϊ���������識���
�е��ĸ���ԭ�ӱ�����ȡ�������ɵĻ������Ϊ���������識���

��1. ���Ľṹ������
1. ���Ľṹ
�������е�ԭ��λ��������ԭ�����ڵ�ƽ���Ϸ����������ӳ����Σ����������Ϊ��

�װ������װ������еļ������Ƿֱ�Ϊ��
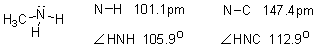
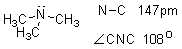
��ˣ�������Ϊ���Ͱ������е�ԭ��λsp3�ӻ����ĸ�sp3�ӻ�����У���һ��Ϊ���Ӷ���ռ�ݣ���������sp3�ӻ�����������̼ԭ��������-�� ��
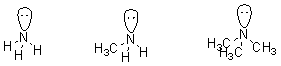
���������м��������ǵ���ֵΪ��
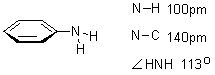
����ƽ����NH2����ԭ������ƽ��֮��ļн�Ϊ142.5O�����װ�������C��N����NH2����ƽ��֮��ļн�Ϊ125O��
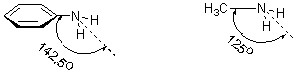
˵���ڱ��������У���ԭ�Ӹ��ӽ���ƽ�湹�ͣ���ԭ�ӵ��ӻ�״̬��sp3��sp2֮�䣬�ȼװ����ӽ���sp2�����ڹµ��Ӷ����ڵĹ�����и����p����ɷ֣������뱽���������ӵĹ���ص���ʹC��N�����в���˫�������ʣ���ˣ�C��N���ļ����ȼװ���C��N���̡������Ľṹ�ù���ʽ��ʾ��Ϊǡ����
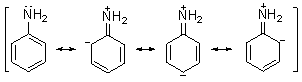
2.����������
�� ��һ��������������д����Nԭ�����������������ƣ�����������β���磺
CH3NH2 �װ�
�� �ԳƵ��ٰ����尷��R��ͬʱ����ȡ��������Ŀ����R������֮ǰ������������β�� �磺
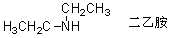
���ԳƵ��ٰ����尷�������̫���ӣ��ɿ����Dz����ĵ�ȡ��������������ѡȡR������ӵ���Ϊĸ�岮�����磺
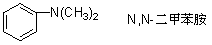
�� ��Ԫ���Ͷ�Ԫ���IJ��������䰷������ֱ��������ֱ�����ڻ���ʱ���ɳ�Ϊ�������������磺
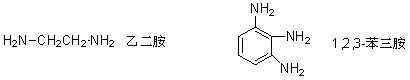
�� �Ƚϸ��ӵİ����ɿ�������������������������������Ϊȡ�������磺
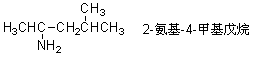
�� �����������Կ�����������������������
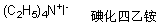
��2. ������������
1.�������ʣ�����ѧ��
2.�������ʣ�
IR: ��һ����R-NH2�����ڶ�����R2NH��������N-H������3500~3300�M-1������N-H�������ա�
RNH2 ����N-H������������շ� 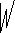 ,��������������N��������ԭ����ɶԳƺͲ��ԳƵ������������� .
,��������������N��������ԭ����ɶԳƺͲ��ԳƵ������������� .
R2NH�� ��һ�����������շ� 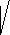
R3N����N-H���������շ塣
�Ͱ���N-H���������շ�����Ͳ����Σ����γ����������N-H������
NMR:-NH-������û��ȷ���Ļ�ѧλ�ƣ�������һ���ܿ��ķ�Χ�ڱ仯���ڵ�һ�͵ڶ����������γ�����̶ȵIJ�ͬ��N-H�Ļ�ѧλ�Ʊ仯�ϴģ�0.6~0.5��
���ĺ˴Ź�������Ҳ�����ڴ����ѣ����ĵ縺�Ա�̼������С������ڰ������нӽ���ԭ�ӵ���Ļ�ѧλ�ƣ����ڴ������нӽ���ԭ�ӵĻ�ѧλ��С���磺
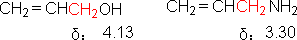
��3. ���������
�������е�ԭ���Ͼ���δ���õĵ��Ӷ�ʱ���ܽ���һ�����ӣ��Գ����ԡ�
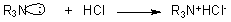
1. ֬������
�л���������ʱ������Һ������ʾ������Բ�ͬ������ʱ�����Ժͼ����Ƿ��ӱ������е����ԣ�������Һ�е����������Ϊ�������ܼ��������һ�����������ǵġ�
i . ��������

��ԭ����Ե���ЧӦ���ͣ���֬�������������γ������Ӻ������������ɵĵ�ԭ�������ļ�����Ϊ�����ӣ���Խ�࣬������Խǿ��������Խ�ȶ������Ĺ�������Խǿ��
ii ��ˮ��Һ�У�
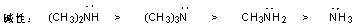
һ����Ϊ�����ǵ���ЧӦ���ܼ����Ľ�����Ӳ������ٰ���������һ���������ڵ���ЧӦ��ʹ�����������ǿ�������ġ������װ��ļ��Է����ȼװ�����������Ϊһ�ְ���ˮ�еļ� �Ȳ���Ҫ��ȡ�����ĵ���ЧӦ����Ҫ�����������Ӻ��γ������ӵ��ܼ����̶ȡ���ԭ����������Խ�ࣨ���ҲԽС��������ˮͨ������ܼ����Ŀ����Ծ�Խ��
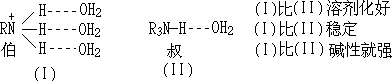
�ڲ������尷֮�䣬�ܼ���ЧӦռ������λ��ʹ�尷���Աȼװ�������
�ο����ף����ӿ�.��ѧ��ѧ��1988��3��3����29
2.�����ļ��ԣ�
���㰷��ˮ��Һ�м��ԱȰ��������ڷ��㰷�е�һ��������ǿ��������������������ǿ��˳��Ϊ��PhNH2��Ph2NH��Ph3N���������ڷ���p,������Ľ������ɱ�����ɢ���ϵĸ���ɡ�ȡ�������ļ���ǿ����ȡ���������ʺ��ڱ����ϵ�λ���йأ����������й����ӻ���ʱ�������������������ӻ�ʱ���Խ��͡��磺

1. ���������
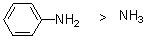
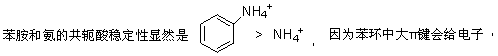
ʹ��ԭ��������ɷ�ɢ��ʹ 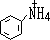 ��
�� 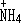 ���ȶ������ԣ��������У������ļ��Դ��ڰ���
���ȶ������ԣ��������У������ļ��Դ��ڰ���
ii . ��ˮ��Һ�м��ԣ�
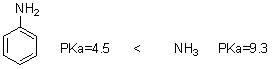
�������ܼ���ЧӦ�����͡�������λ���ʹ 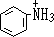 �ܼ����̶�С��
�ܼ����̶�С��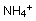 ����ˣ��ܼ�������ʹ
����ˣ��ܼ�������ʹ 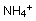 ���ȶ��������ļ�����ˮ�бȱ���ǿ��
���ȶ��������ļ�����ˮ�бȱ���ǿ��
�����ļ��Ա�֬�������Ķࡣ������Ҫ�ǵ�ԭ���ϵ�δ���õ��Ӷ��������ϣ���ԭ�ӵĵ����ܶȼ��٣��������ӵ�������С����ˮ��Һ�� 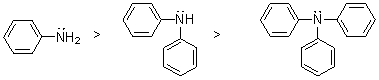
�ܼ���ЧӦ
3. ���ԣ�
�������ٰ��ĵ�ԭ���ϻ����⡣��ʧȥһ�����Ӷ������ԡ�
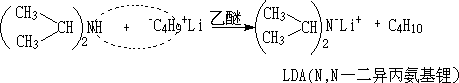
LDA����һ��ǿ�����Լ������л��ϳ��Ϸdz����á���ԭ�ӵĿռ�λ���������λ��С���������á������ܷ��������˷�Ӧ�������ܶ�ȡ��������ֲ����˷�Ӧ��ǿ�����Լ�����Ϊ���˼

LDAֻ��ȡλ��С������H��
4.���ķ��룺
���������ɵ�����ȡ������һ����ˮ���нϴ���ܽ�ȣ���һ���ʿ����ڰ������Ի�����ķ��롣���磺

��4 ���ķ���
1.������
����Ϊ���Լ���±��������SN2��Ӧ����������ڶ��������ͼ���Ρ��ڶ����������ü������������İ���

����κͼ����ò�����ת��Ϊ���� ���ԣ������������ʵ���������õ���һ�����������ͼ���εĻ������ù����IJ�±���飬���Եõ�����Σ�
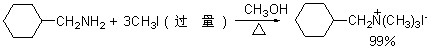
2. ������Ӧ
��Ϊ���Լ���һ��������һ�����ܸ����ȡ�������������������������������ԭ����û����ԭ�ӣ����Բ�������������

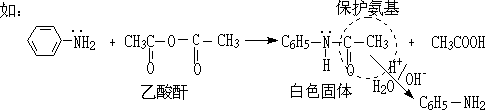
�����Ǿ���һ���۵�Ĺ������ʣ�������ǿ���ǿ���ˮ��Һ�м��Ⱥ�����ˮ�����ɰ�����ˣ����л��ϳ��������Ȱѷ�������������������Ѱ��������������ڽ���������Ӧ��Ȼ��ʹ����ˮ���ڱ�Ϊ����
�� ��˹��(Hinsberg)���飺
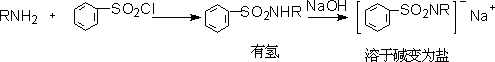
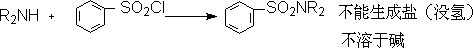
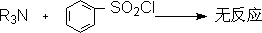
���Գ����ñ�������������������ְ���
3.�����������ã�
�� ֬���壺
��һ��
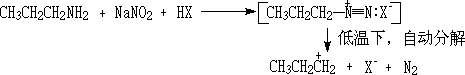
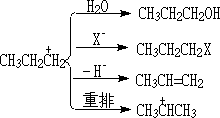
��ˣ������Ӧ���л��ϳ�����;����
�ڶ�����

���������������Ӧ��
�� �����壺
��һ����
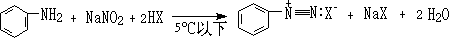
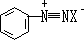 ����֬���ص����ȶ���5�����²��ֽ⣬�������ڷ���̼�����������γɵ�Ե�ʡ�
����֬���ص����ȶ���5�����²��ֽ⣬�������ڷ���̼�����������γɵ�Ե�ʡ�
�ڶ���
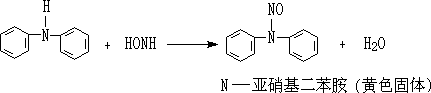
������
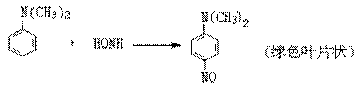
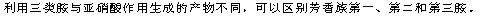
4. ����
���������������������ɷ�Ϊ���ַ�ʽ���С�һ���Ǽ���������һ�������⡣����:
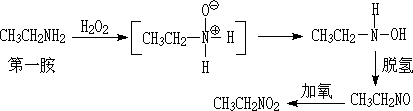
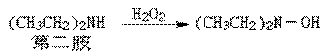
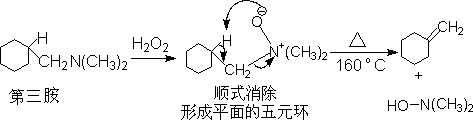
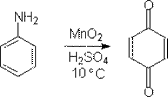
��Ҫ�IJ�����������������ʺ�ʵ��������
�����������ӻ���±�ء�����������ȣ�����������������������������������

N.N-����������ͷ���ζ�����������ô���С���ˣ���ʱ�Ƚ���������κ������ء�
�� ���Ц�-��İ�����������ʱ����������Ӧ����ϩ������һ��Ӧ��A.C.Cope������Ӧ�����ڷ�Ӧ�����γ�ƽ�����Ԫ����������������Ϊ������-��ļ������ͬ��������������רһ�Ե�˳ʽ������
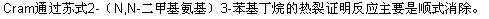
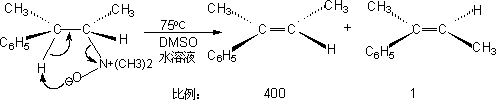
5.±����Ӧ
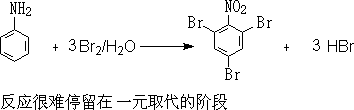
���Ҫ��ȡһ�屽���ͱ���ʹ�����Ļ��Խ��͡�Ҳ����ʹ�����Ļ��Լ��١�
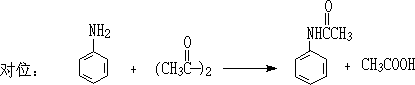
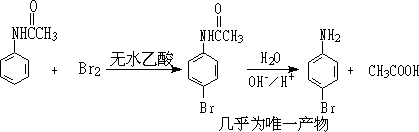
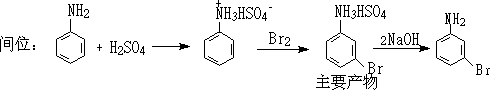
6.�ǻ����ã�
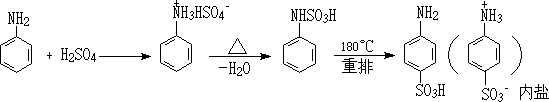
7. �������ã�
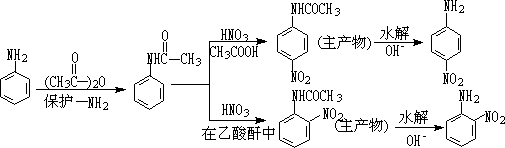
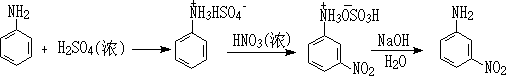
��5�������-�������ط�Ӧ������������������
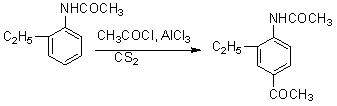
��5. �����Ʒ�
1. ����ֱ������
����Ϊһ�����Լ�������ͬ±����������������SN2��Ӧ���ɲ������Σ�������Ѹ���백��������ת�ƶ��ͳ�������
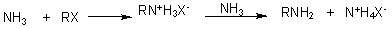
���ַ�����;���ޣ���Ϊ���ɵIJ�����������������Ҳ�����һ�����������ᴿ��һ�����ѡ�
������������������±�����ķ�Ӧ�ڽϸߵ��¶��²��ܽ��У����ɵ��ٰ�Ҫ�ھ��ҵ��¶�С���ܼ�����Ӧ���������ͣ�����ٰ��Ľ� ���磺

2. Gabriel�ϳɷ���
�ڴ˷�������������������������ռ�ݵ�ԭ���������۵�λ�ã�ֻ����һ���ɹ�����ȡ�����⣬��������ȥ���������磺
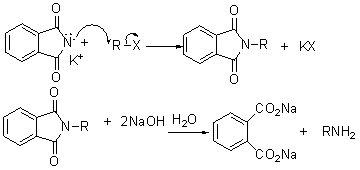
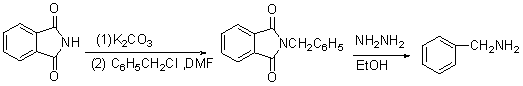
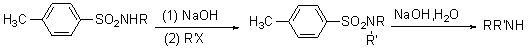
3. ���ط�Ӧ��
�ǰѵ�ԭ���������۶�ռ��������ֻ�����͵ŵ��Ӷԣ�������ˮ�⣬�õ�������
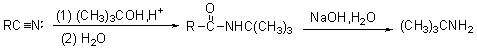
4. ��ԭ����
��̼����������˫�����������Ļ����ﻹԭ�����Եõ�����
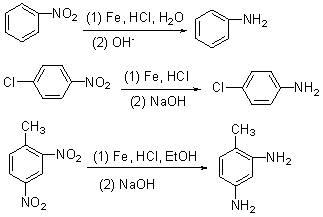
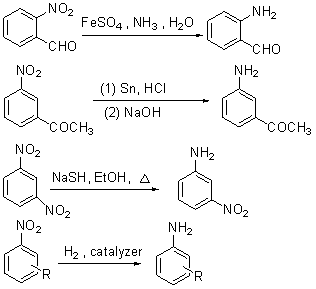


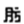 ����ԭ�ɲ�����������ȩͪ�Ʊ������ļ�㷽����
����ԭ�ɲ�����������ȩͪ�Ʊ������ļ�㷽����
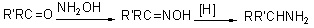
�磺
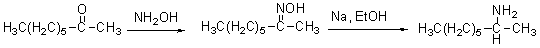

ȩͪ��ԭ��������1��ȩͪ�백��Ӧ�����ǰ����ǰ������������Ϊ������
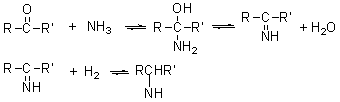
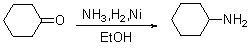
��2��ȩͪ�벮����Ӧ���ȵõ�ϯ���ٴ�����õ��ٰ���
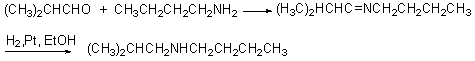
��3��ȩͪ���ٰ�һ������������尷���м����Ϊ����������ˮ���
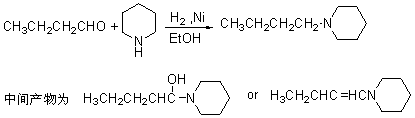
ȩͪ��������ڴ���Һ������������ƣ�NaBH3CN,��ԭ�õ�������
����淋������ǹ�����ʹȩͪת����ǰ����������⻯�Ʒ����е�һ������������Ϊ��ʹ�Լ��Ļ�ԭ�������ͣ�ʹ�䲻�ܽ�ȩͪ��ԭ�ɴ������ֺϳɰ��ķ������ص��Dz������㡣�磺
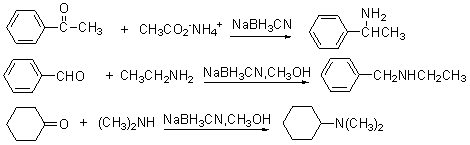
5. ������Hofmann���ţ�
�������Ȼ����ڼ���Һ�з�Ӧ��������һ��̼ԭ�ӣ��ʻ�̼ԭ�ӣ��IJ�������ΪHofmann���š��ڷ�Ӧ�����������е��ʻ�̼ԭ�ӳ�Ϊ̼������ȥ����ˣ�����ʹ̼�����ε�һ�ַ������������ڲ������Ʊ���
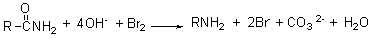
�磺

Hofmann���ſ��ܵĻ���Ϊ��
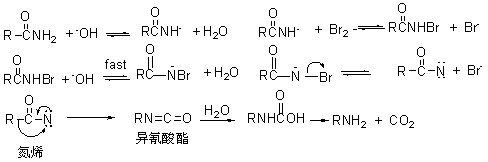
Hofmann�������廯ѧ���������У�Ǩ�Ƶ������Ĺ��ͱ��ֲ��䡣�磺
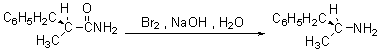
��6.������;
����ѧ��
��7 �����������Ͱ���ȡ����
1. ����
��1��1��1-����
1��1-�������ȶ��Ծ�������ṹ������Ķ�����������δ�õ����������װ�����������ˮ��Һ�����ȶ��ġ���״��1��1-����������ȫ�Ʊ������磺

��������ǽᾧ���壬�ڼ�����Һ�����ȶ��ģ�����������Һ����ˮ���ȩ��
�����Ǽ��İ�Ҳ��һ��1��1-������
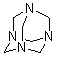
��2���Ҷ������Ʊ���
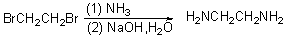
��3��1��6-������ �ϳ�����66��ԭ�ϣ���ҵ�ϳɷ����ǣ�
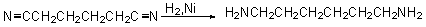
��4���������ĺϳɼ��䷴Ӧ
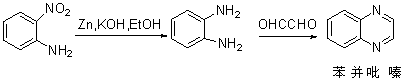
2. ϩ��
ϩ�������е�ԭ��������ԭ��ʱ������ת��Ϊ�ǰ�����ϩ������ת��Ϊ�ʻ����������ƣ�
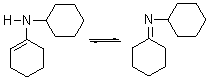
��ϩ�������е�ԭ���������ⶼ������ȡ���������ȶ��Ļ����
ϩ���Ľṹʽ���ù���ʽ��ʾ��
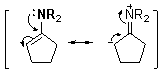
���ڵ�ԭ���ϴ���������ɣ�ϩ���ļ��Ա�����ԭ�ϵİ�������-̼ԭ�����ڴ����ָ���ɶ������ԡ�
ϩ�����Ʊ����÷�����ʹȩͪ���ٰ����ϣ�Ϊ�˼��ٷ�Ӧ�Ľ��У����Լ��뱽���ױ�����ױ������ɵ�ˮ������������Լױ��������������Ҳ������̼���ơ�����ɸ����ˮ���磺
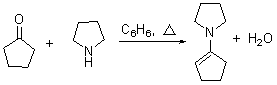
��Ӧ�������£�
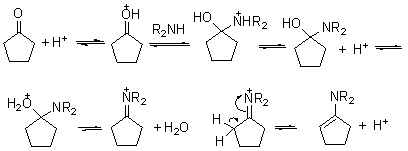
ϩ����±��������ȡ����Ӧ������ˮ���õ���-λ����ͪ��

ϩ����������������ϩ���Ļ����������˶��ӳɷ�Ӧ��
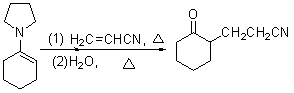
3. �ǻ���
��1���Ҵ������Ʊ���
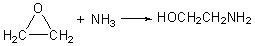
�������������װ���ˮ��Һ��Ӧ�����ɵ����������������һ��������ɶ��Լ������:
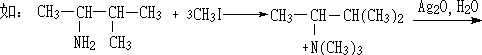
(2) ������ �������ӣ���ǿ��ԭ�ԣ������ˮ��Һ������������������Ӱ�������ɶ��������ӻ�ԭ�õ���

��8.����κ���ת�ƴ�
1.�����
i��識���Ʊ��ͷ�Ӧ
��識������û�Ц�-�⣬����������ȡ����Ӧ��
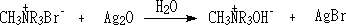
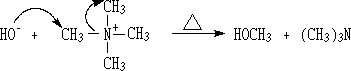
���ĸ�������ͬ�����Ⱥ��������һ��ļ�識���ȷֽ�ʱ���һ����������ϩ���磺

�������������ֻҪ������Ц�-��ԭ�ӣ�����ʱ�ͻ�ʹ�������������ϩ����
ii Hofmann���⣨�˷�Ӧ�������ⶨ���Ľṹ����
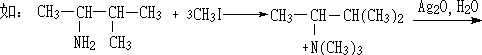
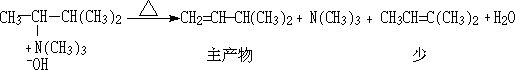
�ⶨһ��δ֪�İ����ӷ�Ӧ���������ĵ�����Ħ����������ϩ���Ľṹ���Ϳ��Ʋ�ԭ���Ļ������ǵڼ�����̼�ĹǼܡ�
�����ù����ĵ�����밷�������ɼ���Σ�Ȼ��ת���ɼ�識����ϩ���ķ�Ӧ��ΪHofmann��������Hofmann ���⡣���ɵIJ�����Ҫ���ڲ�����̼ԭ��������������ٵ�ϩ�������ΪHofmann������һ������Saytze ���������෴��
����識������ڶ��������Խ�������ʱ����-�����������˳�����£�
-CH3>RCH2->R2CH-
iii Ӱ���-����ȥ����������������
��һ���Ǧ�-������ԣ�����Խǿ��Խ����ʧȥ����識E2������Ӧ�����ȷֽ�ʱ�����ڵ�ԭ�Ӵ�����ɣ����ĸ��յ�ЧӦӰ�쵽��-̼ԭ�ӣ�ʹ��-��ԭ�ӵĵ��ӳ��ּ����ܶ��������ͣ��������ӣ��������ܵ������Լ�������
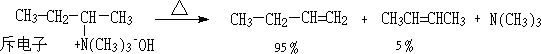
a. �����-̼ԭ�������г���ӻ��ţ�����-̼ԭ�ӵĵ��ӳ��ּ����ܶȵõ����ֲ��䣬�Ӷ�������-������ԣ���-��ԭ��Ҳ�Ͳ����ױ������Լ�������
b. ��-̼���б�������ϩ�����ʻ��������ӻ���ʱ��ʹ��-̼�������ܶȽ��ͣ���-���������ӣ�����������

��һ�����������أ���һ��Ӧ��E2������Ӧ��Ҫ����������Ͱ�������ͬһƽ���ϴ���ȫ����λ�á�����ʽ�������ҹ����ȶ���

��C2-C3���
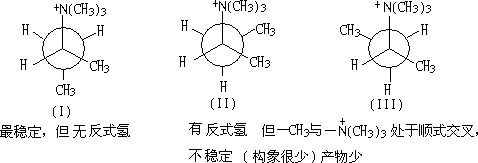
��C1- C2���
��

2. ��ת�ƴ�������ԭ����
��ת�ƴ���ָ��һ�ִ����ܼ��٣�������ʹ�ֱ������ֻ������ܵ��ܼ��е����ʷ�����Ӧ����Ӧʱ��������һ��ʵ�ʲμӷ�Ӧ��ʵ�壬��һ��ת�Ƶ���һ���У��Ա�ʹ���ڵ���������������Ӧ������������̽���ת�ƴ������ã������ִ�������ת�ƴ������磺����Ρ����ѵȡ�
���л��ϳ��г������Ǿ����л���Ӧ�����෴Ӧ���ٶȺ�����Ч����磺 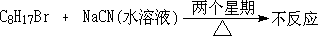
Ҫʹ���Ƿ�����Ӧ����ͳ����÷�����������ʹ���ַ�Ӧ�ﶼ���ܽ���ܼ�������DMSO��DMF��HMPA.����Щ�ܼ���ȱ�������Ǽ۸�ߡ������գ�ͬʱһ������һ��ˮ���Է�Ӧ�ܲ������µĽ���취��Ӧ����ת�ƴ����ã�����������ϵ�м�����������ת�ƴ��������ɴ�������֮��Ľ��棬�ѷ�Ӧʵ�壨-CN����ˮ��ת�Ƶ��л����У�ʹ������RX����Ӧ�����ѷ�Ӧ�е���һ�ָ����Ӵ���ˮ���У�����ת�ƴ���û����ģ�ֻ���ظ�������ת���������ӵ����á�

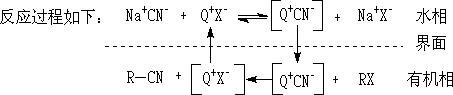
���л����ˮ���ж����ܵ���ת�ƴ�������ˮ�����軯�ƽ��������ӣ�����ý����˸����ӵĴ��������Ӷ���ʽת�Ƶ��л����У��������ԵĴ�����������Q+�Ѹ�����CN-�����л����У��˸��������л������ܼ����̶ȴ�Ϊ��С���������Ӧ���Ժܸߣ���Ѹ�ٵغ͵��RX��������Ӧ������������Ӵ��Ÿ�����X-����ˮ�࣬����������ϵ����ش�������ת�����ӡ�
�ο��� ��������ȡ������л���ѧ��P906-907