第十三章 不饱和醛酮及取代醛酮
§1.α,β-不饱和醛酮
不饱和醛酮分子中,C=C位于α-和β-碳原子间的称谓α,β-不饱和醛酮;位于β-和γ-碳原子间的,则称为β,γ-不饱和醛酮,由于前者和羰基组成共轭体系,所以比后者更稳定。例如:
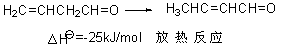
在酸或碱催化下,3-丁烯醛容易转变成2-丁烯醛:
①在碱催化下:
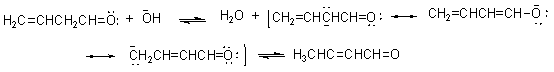 ②在酸催化下:
②在酸催化下:
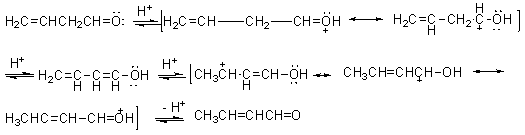
1.α,β-不饱和醛酮 的反应
(1) 亲核加成:
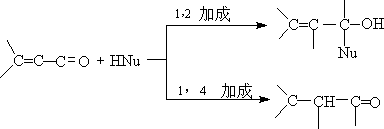
①与HCN加成
α,β不饱和酮与HCN反应,主要生成1,4加成产物:
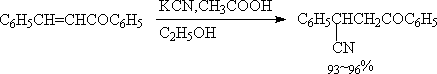
α,β不饱和醛与HCN反应,主要生成1,2加成产物。
② 与格氏试剂加成
羰基上的取代基大小对1,2 和 1,4 加成有一定影响。
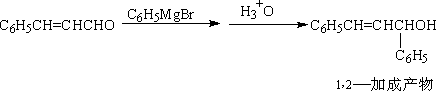
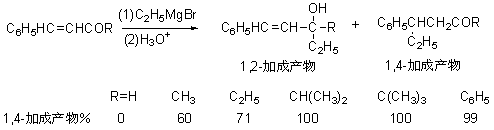
下列反应中的数据也说明了羰基上取代基大小对1,2和1,4 加成的影响:
③与烃基锂加成
主要发生在1,2加成:
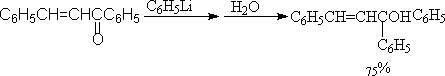
④与二烃基酮锂加成
以1,4 加成为主
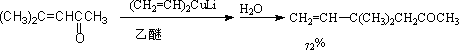
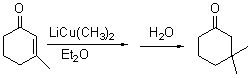
(2)、亲电加成
αβ不饱和醛酮与亲电试剂,一般都发生1,4加成

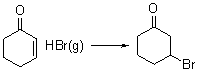
(3)还原
①使羰基还原
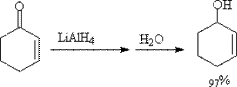
②使双键还原
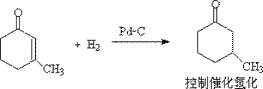
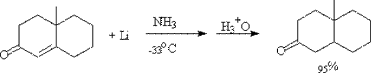
③使羰基,双键同时被还原(催化加氢)
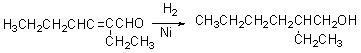
(4)氧化
αβ不饱和醛在温和条件下,可氧化为αβ不饱和羧酸
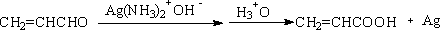
(5)狄尔斯-阿尔德反应(Diels-Alder)反应


2. α,β-不饱和醛酮的制备
有醛酮的缩合反应制备。例如:
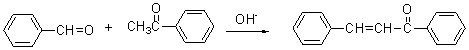
§2. 醌
醌类是一类特殊的环状不饱和二酮,包括一系列化合物,如:
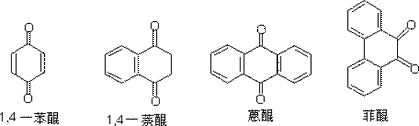
醌类都有颜色。
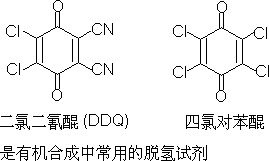
许多动植物来源的有色物质属于醌类,如茜类 。不少生理活性物质是醌类,如维生素K1,就是萘醌的衍生物。
1. 醌的反应
(1)还原 苯醌是一个氧化剂,还原时生成对苯二酚,苯醌和对苯二酚组成一个可逆的电化学氧化-还原体系。

机理:
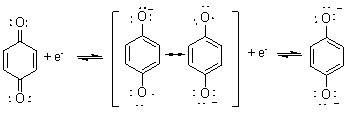
2.加成
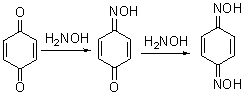
①与羟胺作用:对苯醌与羟胺作用生成一 或二
或二 :(反应必须在酸性溶液中进行,因为在碱性溶液中苯醌可以使羟胺氧化)
:(反应必须在酸性溶液中进行,因为在碱性溶液中苯醌可以使羟胺氧化)
② 与格氏试剂反应,生成醇。
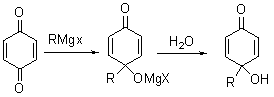
§3. 羟基醛酮
1. 羟基醛酮的反应
(1) α-羟基醛酮其烯醇为烯二醇:
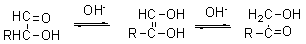
烯二醇也是α-羟基酮的烯醇,因此,α-羟基醛和α-羟基酮可以互变。
α-羟基醛酮与苯肼作用生成脎
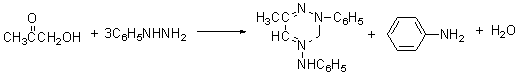
能被高碘酸裂解:
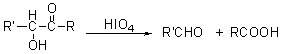
(2) β-羟基醛酮 在酸性溶液中脱水生成α,β-不饱和醛酮,反应速率比一元醇快得多。
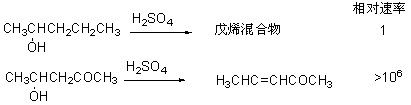
这是由于它们的脱水机理不同:β-羟基醛酮是通过烯醇脱水:
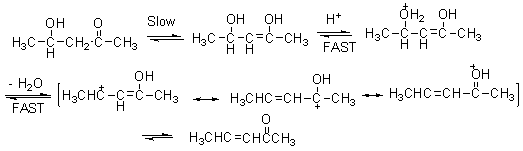 (3)γ-和δ-羟基醛酮它们与环状半缩醛形成动态平衡:
(3)γ-和δ-羟基醛酮它们与环状半缩醛形成动态平衡:
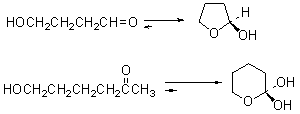
2. 羟基醛共同的制备
(1)1,2-二醇的氧化
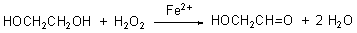
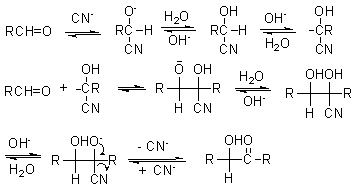
(2)安息香缩合

反应机理:
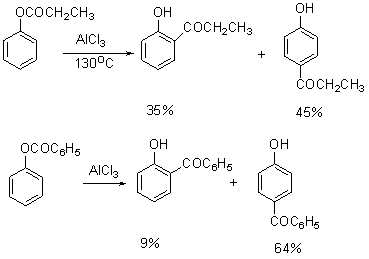
§3 酚醛和酚酮
酚醛和酚酮的合成方法
1. Vilsmeier甲酰化反应
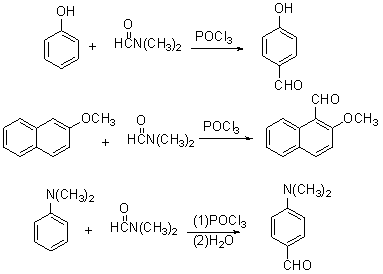
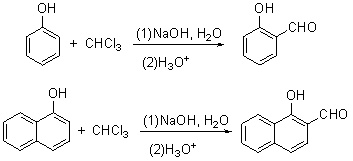
2. Reimer-Tiemann反应
3. Fries重排